آموزش جلسه 1 فصل 2 شیمی دهم بهصورت تستبیس، همراه با تدریس ویدیویی «دکتر متین هوشیار» را، در این پست از رپیتیچ ببینید.
در فصل اول که شامل چهار جلسه بود، با چگونگی پیدایش عنصرها تا مبحث تبدیل اتمها به مولکولها آشنا شدیم. قرار است در اولین قسمت از فصل دو شیمی ده، به بررسی خواص، رفتار و برهم کنش گازها بپردازیم.
خب، اول از همه بریم که ویدیوی آموزشی این بخش رو ببینیم.
آموزش ویدیویی فصل دوم شیمی دهم جلسه 1
در این قسمت، بخشی از «آموزش جلسه اول فصل دوم شیمی دهم» را بهصورت ویدیویی میتوانید ببینید. مدرس این قسمت، آقای دکتر متین هوشیار، رتبه 127 کنکور تجربی هستند.
فرم دریافت آموزش های ویدئویی کامل شیمی:
اگه میخوای کل شیمیت رو تو کمترین زمان و با تدریس انیمیشنی مفهومی تستی رتبه 127 کنکور، آقای دکتر متین هوشیار جمع کنی؛ فرم رو پر کن و منتظر تماسمون باش:
روی نمره 20 و درصد بالای 70 شیمی (مثل رتبه های برتر هر سالمون) حساب کن!
در ابتدا با اتمسفر زمین و ویژگیهای آن آشنا میشویم. پس از آن درصد حجمی گازهای سازنده هوا را بررسی میکنیم. مبحث آخر، به تقطیر جزء به جژء هوای مایع اختصاص دارد.
خواص، رفتار و برهم کنش گازها؛ جلسه 1 فصل 2 شیمی دهم
زمین در فضا مانند گویی فیروزهای، درون هالهای از گازها در چرخش است. اولین وظیفه این هاله سرشار از هوای پاک، نگه داشتن گرمای خورشید در درون خود است. محافظت از ساکنان زمین در برابر پرتوهای خطرناک کیهانی و توزیع آب در سرتاسر سیاره، از دیگر وظایف آن هستند. کره زمین با چرخش خود، باعث تداوم زندگی میشود. برای ادامه زندگی سالم و پایدار، رفتار انسانها با دیگر ساکنان کره باید منطقی باشد. در اصل رفتار ما باید هماهنگ و سازگار با طبیعت باشد و نظم آن را بر هم نزند.
با بررسی خواص، رقتار و برهم کنش گازهای این پوشش آبی رنگ، راههای تداوم زندگی سالم را مییابیم. با کمک گرفتن از علم شیمی، میتوان از به جا گذاشتن ردپای سنگین روی کره زمین جلوگیری کرد.
اتمسفر زمین
در میان سیارههای سامانه خورشیدی، این زمین است که اتمسفر آن امکان زندگی را فراهم میکند. این اتمسفر، مخلوطی از گازهای گوناگون است که تا فاصله 500 کیلومتری از سطح زمین امتداد دارد. میتوان گفت که ما، در کف اقیانوسی از مولکولهای گازی زندگی میکنیم. جاذبه زمین این گازها را پیرامون خود نگه میدارد و مانع از خروج آنها از اتمسفر میشود. انرژی گرمایی مولکولهای گازی، باعث میشود تا پیوسته در حال جنبش باشند و در سرتاسر هواکره توزیع شوند.
اگر زمین را به سیب تشبیه کنیم، ضخامت هواکره نسبت به زمین به نازکی پوست سیب میماند.
اغلب گازها نامرئی هستند. ما هوا را نمیتوانیم ببینیم و به طور معمول وجود آن را در پیرامون خود حس نمیکنیم. اگر باد بوزد یا هوا به خوبی در جریان باشد، میتوان آن را احساس کرد. میان گازهای هوا، واکنشهای شیمیایی گوناگونی رخ میدهد که اغلب آنها برای ساکنان سیاره سودمند هستند. با این حال، برخی از این واکنشها مفید نیستند. این واکنشها فراوردههایی تولید میکنند که دلخواه و مطلوب ساکنان سیاره خاکی نیست.
فشار هواکره
فشار هر گاز، ناشی از برخورد مولکولهای آن با دیواره ظرف است. هواکره هم به دلیل داشتن گازهای گوناگون، فشار دارد.
فشار هواکره در همه جهات بر بدن ما، به میزان یکسان وارد میشود.
با هم بیندیشیم صفحه 47
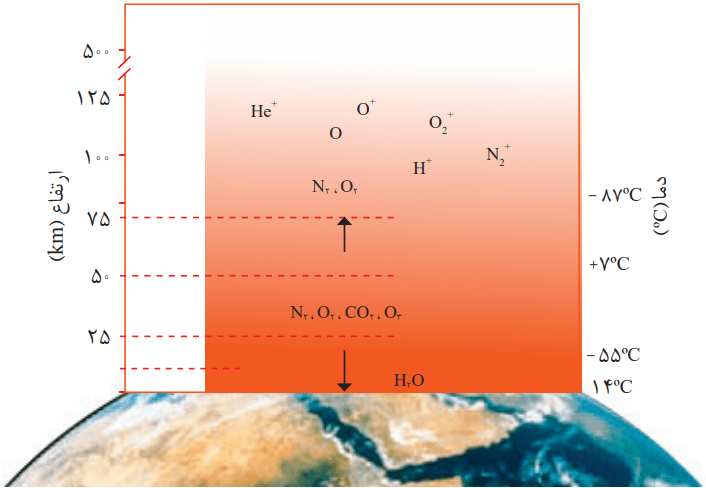
1- در شکل زیر، تغییر دما و برخی اجزای سازنده هواکره بر حسب ارتفاع از سطح زمین نشان داده شده است.
با توجه به این شکل:
آ) آیا روند تغییر دما در هواکره را میتوان دلیلی بر لایهای بودن آن دانست؟ توضیح دهید.
بله. با توجه به نمودار، تفاوت غلظت گازها و روند کاهشی یا افزایش دما میتواند دلیلی بر لایهای بودن هواکره باشد. انواع مختلفی از مولکولها در لایههای مختلف موجودند. برای مثال در لایه استراتوسفر، غلظت مولکول O3 بیشتر است. با افزایش ارتفاع در پایینترین لایه، دما کاهشی است. در لایه بعدی، دما افزایشی است و سپس در لایه بعدی، باز دما کاهشی میشود.
ب) آیا به جز اتم و مولکول، ذرههای دیگری هم در این لایهها هست؟ علت ایجاد آنها را توضیح دهید.
بله، در لایه یونوسفر یونهای مثبت نیز وجود دارند. این یونها در اثر برخورد پرتوهای پرانرژی خورشید با اتمها به وجود میآیند.
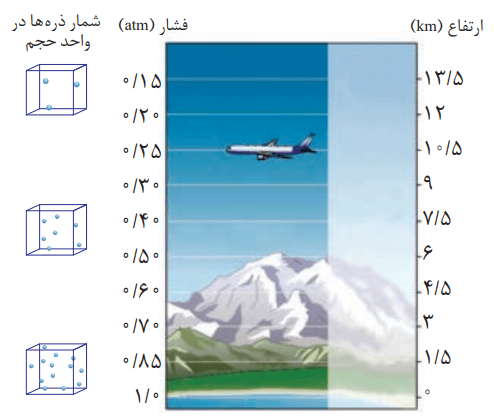
2- دما و فشار هواکره، از جمله عوامل مهم در تعیین ویژگیهای آن است.
با توجه به شکل بالا مشخص کنید که با افزایش ارتفاع از سطح زمین، فشار هوا چه تغییری میکند؟ توضیح دهید.
با افزایش ارتفاع از سطح زمین، فشار هوا کاهش مییابد. این امر به خاطر آن است که تراکم مولکولهای هوا کمتر و هوا رقیقتر میشود.
پیوند با ریاضی صفحه 48
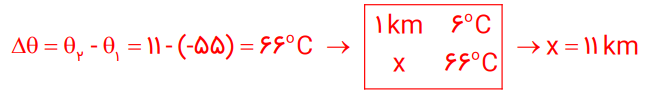
تغییر آب و هوای زمین، در لایه تروپوسفر رخ میدهد. در این لایه با افزایش ارتفاع به ازای هر کیلومتر، دما در حدود 6 درجه سانتیگراد افت میکند. کاهش دما در انتهای لایه به حدود 55- درجه سانتیگراد (218 کلوین) میرسد. اگر میانگین دما در سطح زمین در حدود 14 درجه سانتیگراد (287 کلوین) در نظر بگیریم:
آ) ارتفاع تقریبی لایه تروپوسفر را حساب کنید.
ب) رابطهای برای تبدیل دما، بر حسب درجه سلسیوس به دما بر حسب کلوین پیدا کنید.
K = θ + 273
هوا، معجونی ارزشمند
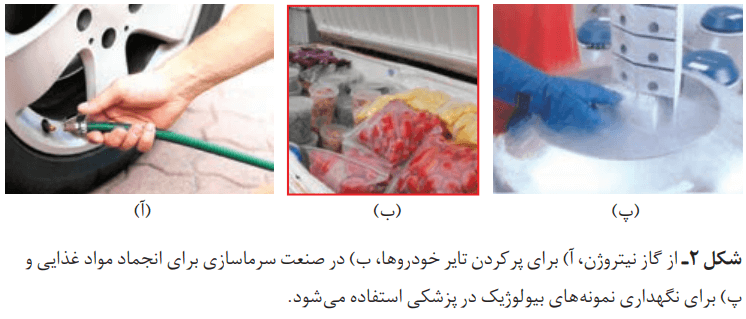
احتمالا تجربه کردید که گاهی مغز گردو، بادام، آفتابگردان و … بو و مزه کهنگی میدهد. دلیل این ویژگی، ماندن آنها در هوای آزاد به مدت طولانی است. در صنعت با بستهبندی مناسب، میتوان زمان ماندگاری مواد غذایی را افزایش داد. جالب است بدانید که در بستهبندی برخی مواد خوراکی از گاز نیتروژن استفاده میشود. کاربردهای دیگر گاز نیتروژن را میتوانید در شکلهای زیر ببینید.
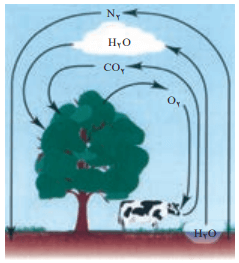
برهم کنس هواکره با زیست کره
زندگی جانداران گوناگون در زیست کره با گازهای موجود در هوا، گره خورده است. گیاهان با بهرهگیری از نور خورشید و مصرف کربن دی اکسید هوا کره، اکسیژن مورد نیاز جانداران را تولید میکنند.
جانداران ذرهبینی، گاز نیتروژن هواکره را برای مصرف گیاهان در خاک، تثبیت میکنند.
نیتروژن، اکسیژن و کربن دی اکسید، از جمله گازهای هواکره هستند که در زندگی روزانه نقش حیاتی دارند.
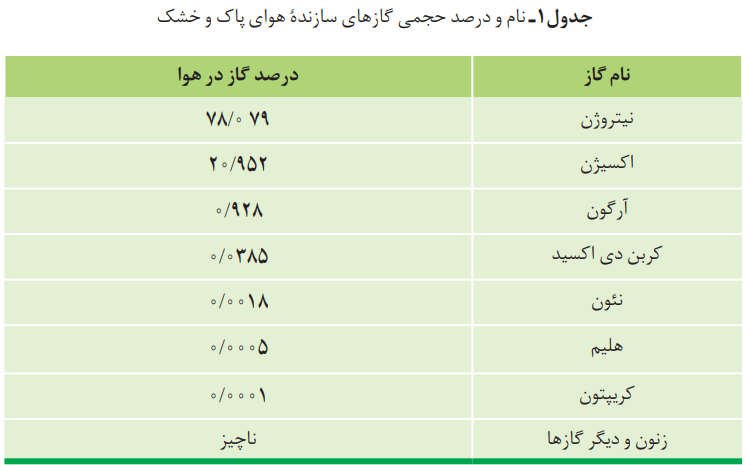
درصد حجمی گازهای سازنده هوا
آیا هواکره میتواند منبع ارزشمندی برای تهیه برخی گازها باشد؟ حدود 75 درصد از جرم هواکره، در نزدیکترین لایه به زمین (تروپوسفر) قرار دارد. این بخش از هواکره، همان بخشی است که ما در آن زندگی میکنیم. پس از تروپوسفر، هواکره رقیق و رقیقتر میشود. درصد حجمی گازهای تشکیل دهنده هوای خشک و پاک در لایه تروپوسفر را در جدول 1 میتوانید مشاهده کنید. توجه کنید که رطوبت هوا متغیر بوده و میانگین بخار آب در هوا، حدود یک درصد است. این مقدار از جایی به جای دیگر، از روزی به روز دیگر و حتی از ساعنی به ساعت دیگر تغییر میکند.
تقطیر جزء به جزء هوای مایع
بخش عمده هواکره را دو گاز نیتروژن و اکسیژن تشکیل میدهد. گاز آرگون در میان اجزای هواکره، در رتبه سوم قرار دارد. بنابراین، میتوان هوا را منبعی غنی برای تهیه این گازها دانست. در صنعت، این گازها را از تقطیر جزء به جزء هوای مایع تهیه میکنند.
در این فرایند، نخست هوا را از صافیهایی عبور میدهند تا گرد و غبار آن گرفته شود. سپس با استفاده از فشار، دمای هوا را پیوسته کاهش میدهند. با کاهش دمای هوا تا صفر درجه سانتیگراد، رطوبت هوا بهصورت یخ از آن جدا میشود. در دمای 78- درجه سانتیگراد، گاز کربن دی اکسید هوا نیز به حالت جامد در میآید. با سرد کردن بیشتر تا دمای 200- درجه سانتیگراد، مخلوط بسیار سردی از چند مایع پدید میآید. به این مخلوط، هوای مایع میگویند. در مرحله آخر، هوای مایع را از یک ستون تقطیر عبور میدهند. با این کار، گازهای سازنده جداسازی و در ظرفهای جدا ذخیره میشوند.
ویژگی و کاربردهای آرگون
آرگون گازی بیرنگ، بیبو و غیر سمی است. واژه آرگون به معنای تنبل است؛ زیرا واکنشپذیری ناچیزی دارد.
این گاز در پتروشیمی شیراز، از تقطیر جزء به جزء هوای مایع با خلوص بسیار زیاد تهیه میشود.
گاز آرگون اغلب به عنوان محیط بی اثر شناخته میشود. از این گاز در جوشکاری، برش فلزها و ساخت لامپهای رشتهای استفاده میشود.
با هم بیندیشیم صفحه 50
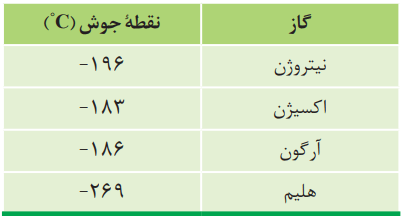
با توجه به جدول، به پرسشها پاسخ دهید:
آ) نمونهای از هوای مایع با دمای 200- درجه سانتیگراد تهیه شده است. اگر این نمونه تقطیر شود، ترتیب جداسازی گازها را مشخص کنید.
گازها بر اساس نقطه جوش از هم جدا میشوند. هرکدام نقطه جوش پایینتری داشته باشند، زودتر جدا میشوند. در این رابطه، هلیم یک استثنا است. این گاز، در هوای مایع با دمای 200- درجه سانتیگراد، بهصورت مایع وجود ندارد.
1- هلیم 2- نیتروژن 3- آرگون 4- اکسیژن
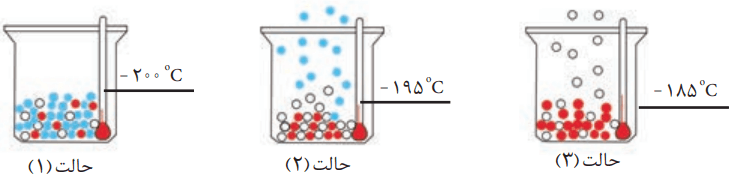
ب) دانشآموزی جداشدن برخی گازها را از هوای مایع، مطابق شکل زیر طراحی کرده است. مشخص کنید هر گوی رنگی، نشاندهنده کدام گاز است؟ چرا؟
گوی آبی، نیتروژن است. با توجه به حالت (2) در دمای 195- درجه سانتیگراد از هوای مایع جدا شده است.
گوی سفید، آرگون است. با توجه به حالت (1) در دمای 185- درجه سانتیگراد از هوای مایع بخار شده است.
گوی قرمز، اکسیژن است. دمای جوش اکسیژن 183- درجه سانتیگراد است. بنابراین در دماهای پایینتر از 183- درجه سانتیگراد هنوز در حالت مایع است.
پ) در دمای 80- درجه سانتیگراد، اجزای سازنده هوای مایع به کدام شکل وجود دارند؟ چرا؟
به شکل گازی (حالت 1) وجود دارند. دلیل آن این است که در این دما هر سه گاز، به نقطه جوش خود رسیدهاند.
ت) توضیح دهید چرا تهیه اکسیژن صددرصد خالص در این فرایند، دشوار است؟
چون نقطه جوش اکسیژن نزدیک به نقطه جوش آرگون و نیتروژن است. در فرایند تقطیر، همواره مقداری از این گازها به همراه اکسیژن، از برج تقطیر خارج میشوند.
پیوند با صنعت صفحه 51
هلیم به عنوان سبکترین گاز نجیب، بیرنگ و بیبو است. از کاربردهای فراوان این گاز، میتوان به موارد زیر اشاره کرد:
- پرکردن بالنهای هواشناسی، تفریحی و تبلیغاتی
- استفاده در جوشکاری
- بهکارگیری در کپسول غواصی
- خنککردن قطعات الکترونیکی در دستگاههای تصویربرداری مانند MRI
هلیم در کره زمین به مقدار خیلی کم یافت میشود. مقدار ناچیزی از آن در هوا و مقدار بیشتری در لایههای زیرین پوسته زمین وجود دارد. بنابراین منابع زمینی آن از هواکره سرشارتر و برای تولید هلیم در مقیاس صنعتی مناسبترند.
گاز هلیم از واکنشهای هستهای در ژرفای زمین تولید میشود. این گاز پس از نفوذ به لایههای زمین، وارد میدانهای گازی میشود.
یافتههای تجربی نشان میدهد که حدود 7 درصد حجمی از مخلوط گاز طبیعی را هلیم تشکیل میدهد. البته مقدار هلیم در میدانهای گازی گوناگون، متفاوت است.
هلیم را میتوان افزون بر هوای مایع، از تقطیر جزء به جزء گاز طبیعی نیز بهدست آورد. تهیه این گاز از کدام روش مقرون به صرفهتر است؟ چرا؟
تهیه هلیم از گاز طبیعی به صرفهتر است. درصد حجمی هلیم در گاز طبیعی، نسبت به هوا خیلی بیشتر است. با این حال، تقطیر جزء به جزء گاز طبیعی برای استخراج هلیم، نیاز به تکنولوژی بالایی دارد.
جداسازی هلیم از گاز طبیعی، به دانش و فناوری پیشرفتهای نیاز دارد. متخصصان کشورمان تا کنون، موفق به جداسازی و تهیه آن نشدهاند. همچنان، هلیم از دیگر کشورها وارد میشود.
فرم دریافت آموزش های ویدئویی کامل شیمی:
اگه میخوای کل شیمیت رو تو کمترین زمان و با تدریس انیمیشنی مفهومی تستی رتبه 127 کنکور، آقای دکتر متین هوشیار جمع کنی؛ فرم رو پر کن و منتظر تماسمون باش:
روی نمره 20 و درصد بالای 70 شیمی (مثل رتبه های برتر هر سالمون) حساب کن!
برای دسترسی به دیگر درسهای فصل 2 شیمی 10، روی لینک های زیر کلیک کنید: