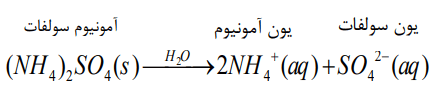آموزش جلسه 1 فصل 3 شیمی دهم بهصورت تستبیس، همراه با تدریس ویدیویی «دکتر متین هوشیار» را، در این پست از رپیتیچ ببینید.
در فصل اول، با اتمها، عنصرها و یونها و در فصل دوم با گازها آشنا شدیم. حال در فصل آخر قرار است که با آب، این مایه حیاتبخش روبهرو شویم. در اولین جلسه از فصل سوم به بررسی مباحث ابتدایی محلول و آشنایی با یونهای چند اتمی میپردازیم.
خب، اول از همه بریم که ویدیوی آموزشی این بخش رو ببینیم.
آموزش ویدیویی فصل سوم شیمی دهم جلسه 1
در این قسمت، بخشی از «آموزش جلسه اول فصل سوم شیمی دهم» را بهصورت ویدیویی میتوانید ببینید. مدرس این قسمت، آقای دکتر متین هوشیار، رتبه 127 کنکور تجربی هستند.
فرم دریافت آموزش های ویدئویی کامل شیمی:
اگه میخوای کل شیمیت رو تو کمترین زمان و با تدریس انیمیشنی مفهومی تستی رتبه 127 کنکور، آقای دکتر متین هوشیار جمع کنی؛ فرم رو پر کن و منتظر تماسمون باش:
روی نمره 20 و درصد بالای 70 شیمی (مثل رتبه های برتر هر سالمون) حساب کن!
در ابتدا با چرخه آب در کره زمین آشنا میشویم. پس از آن همراهان ناپیدای آب، که شامل یونهای تک اتمی و چند اتمی میشوند را بررسی میکنیم. مبحث آخر، به محلول و مقدار حل شوندهها اختصاص دارد.
چرخه آب در کره زمین؛ جلسه 1 فصل 3 شیمی دهم
زمین در فضا به رنگ آبی دیده میشود؛ زیرا حدود 75 درصد سطح آن را آب پوشانده است. جرم کل آبهای روی کره زمین در حدود 1018*1.5 تن برآورد میشود. بخش عمده این آب در اقیانوسها و دریاها توزیع شده است. اگر کره زمین را مسطح در نظر بگیریم آب، همه سطح آن را تا ارتفاع بیش از 2 کیلومتر میپوشاند.
آب اقیانوسها و دریاها مخلوطی همگن است که اغلب مزهای شور دارد. دلیل آن، حل شدن مقدار قابل توجهی از نمکهای گوناگون در دل آن است. طبق بررسیها حدود 1016*5 تن نمک در آب اقیانوسها و دریاها وجود دارد. علاوه بر آن، سالانه میلیاردها تن مواد گوناگون از سنگ کره نیز وارد آب میشود. جرم کل مواد حل شده در آبهای کره زمین، تقریبا ثابت است. با این حساب، همین مقدار ماده نیز از آب دریاها و اقیانوسها باید خارج شود.
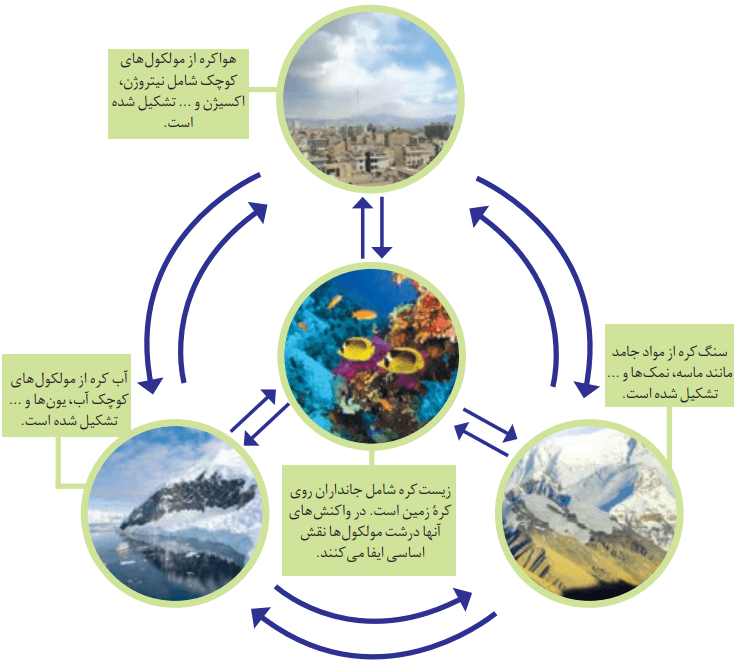
چهار بخش سامانه زمین
کره زمین را میتوان سامانهای بزرگ در نظر گرفت. این سامانه شامل چهار بخش هواکره، آب کره، سنگ کره و زیست کره است.
زمین از دیدگاه شیمیایی پویاست. بخشهای گوناگون آن با یکدیگر برهم کنشهای فیزیکی و شیمیایی دارند.
درون این سامانه و بین چهار بخش، پیوسته مواد گوناگونی مبادله میشود. سالانه حجم زیادی از آب دریاها بخار و وارد هواکره میشود. این آب بهصورت بارش در آب کره یا سنگ کره فرود میآید. جانداران آبزی سالانه میلیاردها تن کربن دی اکسید را وارد هواکره میکنند. در کنار آن، مقدار بسیار زیادی از گاز اکسیژن محلول در آب را مصرف میکنند. فعالیتهای آتشفشانی سبب میشود گازهای گوناگون و مواد شیمیایی جامد بهصورت گرد غبار وارد هواکره شوند.
لاشه جانوران و گیاهان بر اثر واکنشهای شیمیایی تجزیه میشوند. پس از این مرحله، بهصورت مولکولهای کوچکتری وارد آب کره، هواکره یا سنگ کره میشوند. جانداران سالانه مقدار بسیار زیادی از ترکیبهای کربندار را وارد بخشهای گوناگون کره زمین میکنند.
خود را بیازمایید صفحه 87
اولین خود را بیازمایید جلسه اول فصل سوم، دارای 4 سوال است. در ادامه به بررسی آنها میپردازیم و پاسخ هر کدام را میآوریم.
سوال 1
در مورد مواد موجود در آب دریا، به پرسشهای زیر پاسخ دهید:
آ) چند نمونه از این مواد را نام ببرید.
اکسیژن، سدیم کلرید، منیزیم کلرید، کلسیم برمید و …
ب) این مواد از کجا میآیند؟ توضیح دهید.
از سنگ کره و هوا کره. از هوا کره فقط اکسیژن میآید. دیگر مواد محلول در آب، در مسیر رودها و رودخانهها تا رسیدن به دریا، در آب حل میشوند. گاهی برخی مواد از فاضلابهای خانگی و صنعتی نیز همراه آنها به دریا وارد میشود. موجودات زنده در دریا نیز، خود تولید کننده برخی از این مواد هستند.
سوال 2
این عبارت را که «زمین از دیدگاه شیمیایی پویاست» توضیح دهید.
این جمله نشان میدهد که در زمین، پیوسته مواد شیمیایی گوناگون در یک چرخه طبیعی مبادله میشوند. این مواد در میان هواکره، زیست کره، سنگ کره و آب کره در حال جابجایی و تبدیل شدن دائمی به یکدیگرند.
سوال 3
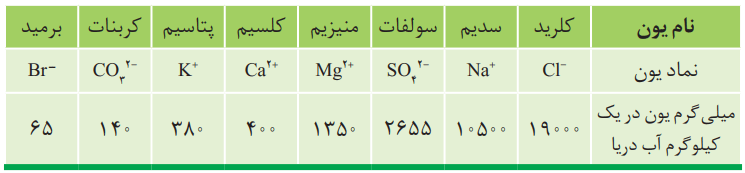
در جدول زیر نام، نماد شیمیایی و مقدار برخی یونهای حل شده در آب دریا را میبینید.
آ) کاتیون عنصرهای کدام گروههای جدول دورهای در آب دریا وجود دارند؟
گروه 1 و 2
ب) مقدار کدام آنیون در آب دریا، از دیگر آنیونها بیشتر است؟
–Cl (یون کلرید)
پ) مقدار کدام کاتیون در آب دریا، از دیگر کاتیونها بیشتر است؟
+Na (یون سدیم)
ت) وجود انواع یونها در آب دریا، به دلیل انحلال نمکهای گوناگون در آن است. نام و فرمول چند ترکیب شیمیایی دوتایی را بنویسید که انحلال آنها باعث ورود یونهای کلرید و سدیم در آب دریا میشود.
NaBr، MgCl2، KCl، CaCl2 و NaCl
سوال 4
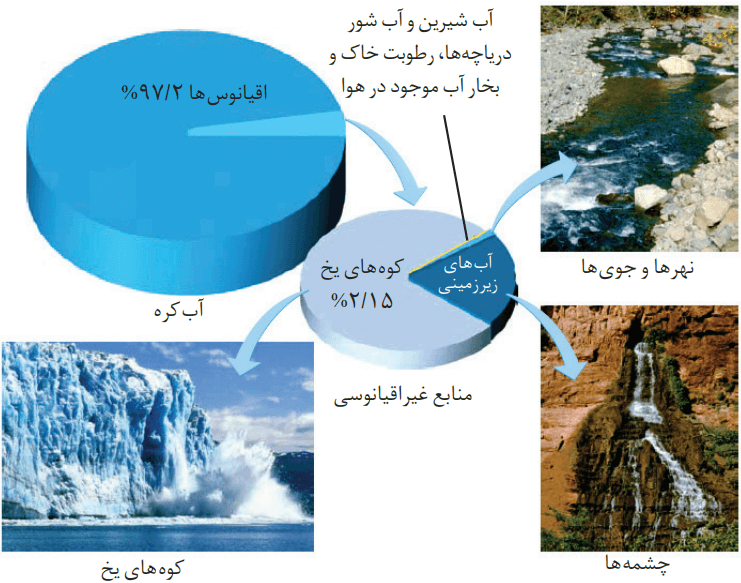
هفتاد و پنج درصد سطح زمین را آب پوشانده است. با این حال 50 درصد جمعیت جهان از کمآبی رنج میبرند. تا سال 2025 چیزی حدود 66 درصد از مردم جهان، با کمبود آب روبهرو خواهند شد. با توجه به شکل، دلیل کمبود آب برای مردم جهان را توضیح دهید.
میدانیم که قسمت عمده سطح زمین را آب پوشانده است. با این حال تنها مقدار ناچیزی در حدود 0.65 درصد از آن را آب شیرین و قابل شرب و کشاورزی تشکیل میدهد. به همین دلیل میگوییم که آب، مایعی کم یاب در عین فراوانی است.
خواص فیزیکی و شیمیایی آب
بیشتر آبهای روی زمین شور است و نمیتوان از آنها در کشاورزی، مصارف خانگی و صنعتی استفاده کرد. تهیه آب شیرین و آشامیدنی و آب قابل استفاده در کشاورزی و صنعت، از چالشهای اساسی در سطح جهان است. اقیانوسها، دریاها و دریاچهها دارای منابع ارزشمندی هستند. از این منابع برای تهیه و استخراج مواد شیمیایی گوناگون، تولید فراوردههای پروتئینی، مواد و وسایل تزئینی، تهیه داروهای گوناگون و … استفاده میشود. با این حساب باید با افزایش دانش شیمی، بتوان پاسخ پرسشهای زیر را پیدا کرد.
- خواص فیزیکی و شیمیایی آب چیست؟
- چرا برخی نمکها در آب دریا حل میشوند، اما برخی دیگر حل نمیشوند؟
- آیا مواد شیمیایی موجود در آب دریا با یکدیگر، آبزیان و جانداران دریایی واکنش میدهند؟
- مواد حل شده در آب دریا از کجا میآیند؟
- کدام ویژگی آب سبب شده است تا زندگی در آب کره در زمستان و با وجود یخ زدن آب ادامه یابد؟
امید است که با آموزش شیمی، شهروندان آگاه با تکیه بر دانش، از منابع خدادادی بهطور مناسب استفاده کنند. در عین حال از ایجاد ردپاهای سنگین و بزرگ بر روی بخشهای گوناگون کره زمین جلوگیری نمایند.
همراهان ناپیدای آب
دریاها مخلوطی همگن از انواع یونها و مولکولها در آب هستند. نوع و مقدار مواد حل شده در دریاها با یکدیگر تفاوت دارند. آبهایی که به دریا میریزند، در مسیر خود از زمینهایی گذر میکنند که مواد شیمیایی گوناگونی دارند.
اغلب چشمهها، قناتها و رودخانهها، آبی زلال و شفاف دارند که شیرین، گوارا و آشامیدنی است. آیا این آبها خالصاند یا ناخالص؟ آیا آبهای معدنی که از رشته کوههای البرز و زاگرس تهیه میشوند، ناخالصی دارند؟
آب آشامیدنی، مخلوطی زلال و همگن بوده که حاوی مقدار کمی از یونهای گوناگون است. برخی از این یونها بهطور طبیعی در آب حل شدهاند. برخی دیگر از آنها در مراکز تامین آب آشامیدنی سالم، به آب اضافه میشوند. مثلا مقدار بسیار کم و مناسبی از یون فلوئورید، به آب آشامیدنی اضافه میشود. وجود این یون، سبب حفظ سلامت دندانها میشود.
در برخی از آبهای آشامیدنی، مقدار یونهای حل شده بهقدری زیاد است که مزه آب را تغییر میدهد. تفاوت آب آشامیدنی و دیگر آبها، در نوع و مقدار حل شوندههای آنهاست.
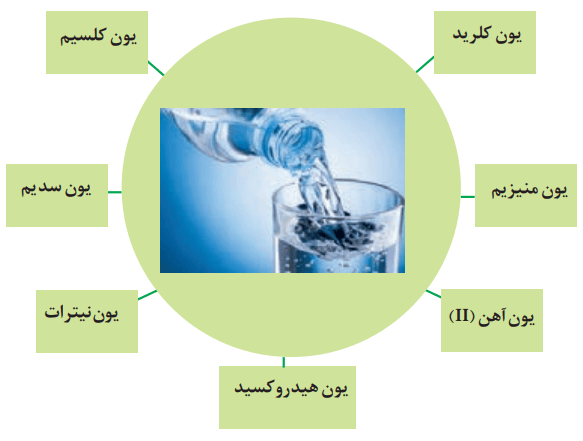
در تصویر بالا، برخی یونهای موجود در آبهای آشامیدنی و شیرین را مشاهده میکنید. مقدار و نوع یونهای موجود در آبهای شیرین از محلی به محل دیگر تفاوت دارد.
یونهای تک اتمی و چند اتمی
برخی از یونهای موجود در آب آشامیدنی، تک اتمی هستند. بعضی از آنها از این قرار هستند:
- +Ca2
- –Cl
- +Na
- –F
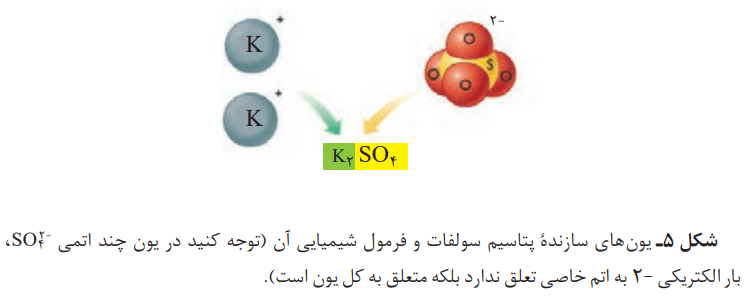
برخی دیگر هم مانند یون نیترات و یون سولفات، از چند اتم تشکیل شدهاند. این یونها را یونهای چند اتمی مینامند. پتاسیم سولفات، ترکیبی یونی است. هر واحد آن شامل دو یون تک اتمی پتاسیم و یک یون چند اتمی سولفات است.
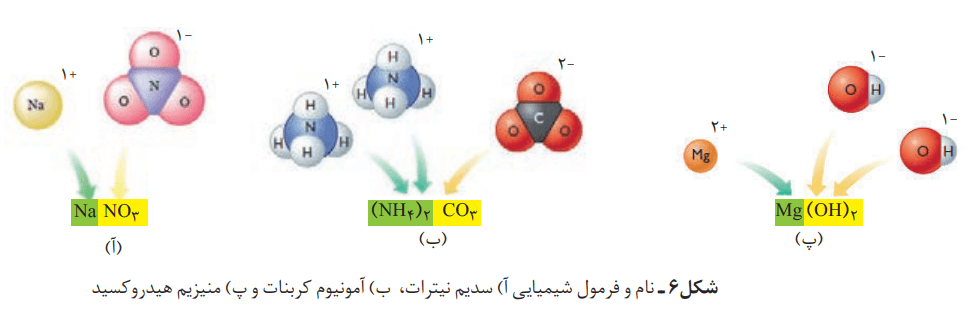
برای نوشتن فرمول شیمیایی این ترکیبها باید به این شکل عمل کرد. نخست نماد کاتیون را سمت چپ و فرمول شیمیایی آنیون را در سمت راست مینویسند. با توجه به اینکه یک ترکیب یونی خنثی است، بر این اساس شمار کاتیونها و آنیونها را مشخص میکنند. پس از آن بهصورت زیروند در سمت راست هر یون قرار میدهند.
خود را بیازمایید صفحه 92
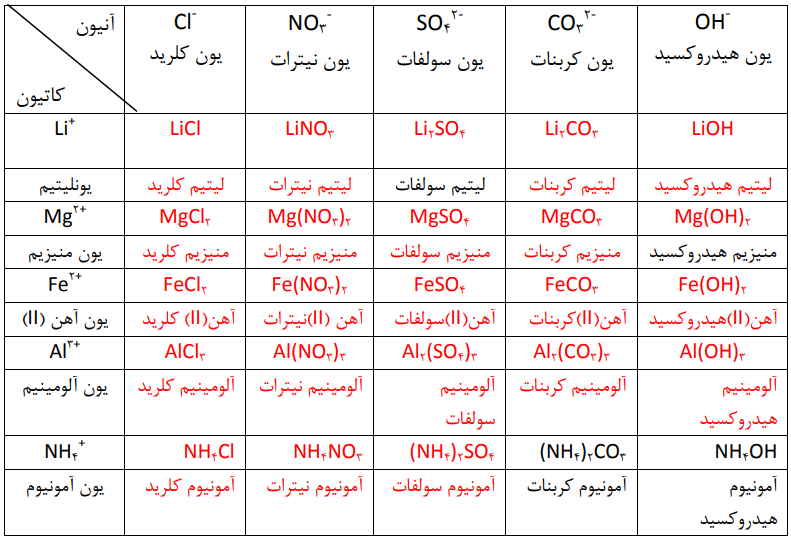
1- جدول زیر را کامل کنید.
جدولی که در صفحه 92 شیمی دهم آمده است، بهصورت زیر کامل میشود.
2- گیاهان برای رشد مناسب، افزون بر CO2 و H2O به عنصرهایی مانند N، P، S و … نیاز دارند. آمونیومسولفات یکی از کودهای شیمیایی است که دو عنصر نیتروژن و گوگرد را در اختیار گیاه قرار میدهد.
آ) از انحلال هر واحد آمونیومسولفات در آب، چند یون تولید میشود؟ توضیح دهید.
از انحلال هر واحد آن، سه یون (شامل دو کاتیون آمونیوم و یک آنیون سولفات) تولید میشود. ضمن انحلال نمک در آب، سمت چپ آن به یون مثبت و سمت راست آن به یون منفی تبدیل میشود. زیروندها به ضریب و بار الکتریکی به توان یون تبدیل میشود.
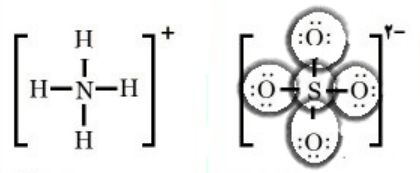
ب) ساختار لوویس یونهای آمونیوم و سولفات را رسم کنید.
محلول و مقدار حل شوندهها
محلول، مخلوطی همگن از دو یا چند ماده بوده که حالت فیزیکی و ترکیب شیمیایی در سرتاسر آن یکسان و یکنواخت است. محلولها کاربردهای فراوانی در زندگی ما دارند که چند نمونه از آنها در شکل پایین آمده است.
عکس
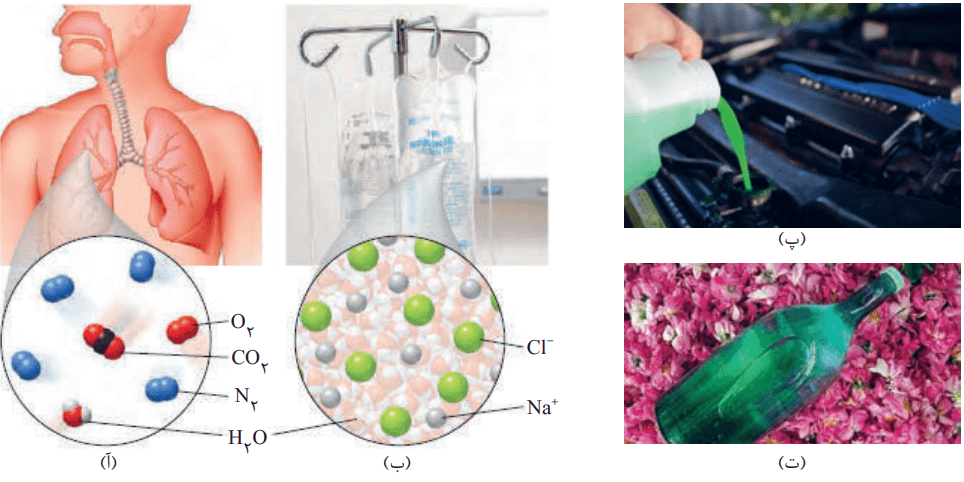
آ) هوای پاکی که تنفس میکنیم، محلولی از گازهاست.
ب) سرم فیزیولوژی محلول نمک در آب است.
پ) ضد یخ، محلول اتیلن گلیکول در آب است.
ت) گلاب مخلوطی همگن از چند ماده آلی در آب است.
در محلول آبی ضد یخ، حالت فیزیکی در سرتاسر آن مایع و ترکیب شیمیایی مانند رنگ، غلظت و … در سرتاسر آن یکسان و یکنواخت است.
برخی محلولها مانند سرم فیزیولوژی رقیق و برخی مانند گلاب دو آتشه غلیظ هستند. هنگامی که میگوییم محلولی غلیظ است، یعنی مقدار حل شونده(ها) در آن زیاد است. گاهی اوقات موقع خوردن صبحانه، حس میکنید که چای شیرین خیلی غلیظ است. این جمله به دو صورت برداشت میشود. یا مقدار شکر موجود در چای زیاد بوده و یا چای بسیار پررنگ بوده است.
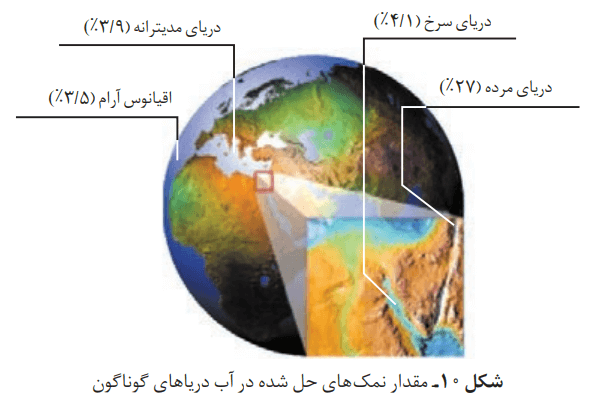
مقدار نمکهای حل شده در آب دریاهای گوناگون
مقدار نمکهای حل شده در آب دریاهای گوناگون، با همدیگر تفاوت دارد.
در هر 100 گرم از آب دریای مرده (بحرالمیت)، حدود 27 گرم حل شونده (انواع نمکها) وجود دارد. از اینرو آب این دریا محلول غلیظی است که انسان میتواند به راحتی روی آن شناور بماند.
دریاچه ارومیه نیز یکی از دریاچههای شور دنیاست که مقدار نمکهای حل شده در آن بسیار زیاد است. محلول آبی این دریاچه نیز بسیار غلیط است. از اینرو دریاچه ارومیه، منبع غنی از مواد شیمیایی گوناگون بهشمار میآید.
غلظت محلول
هر محلول از دو جزءِ خلال و حلشونده تشکیل شده است. حلال جزئی از محلول است که حلشونده را در خود حل میکند و شمار مولهای آن بیشتر است. خواص محلولها به خواص حلال، حلشونده و مقدار هر یک از آنها بستگی دارد. اینکه چه مقدار حل شونده در یک محلول وجود دارد، میتواند به درک خواص، رفتار و کاربرد آن محلول کمک کند.
شیمیدانها غلظت یک محلول را مقدار حلشونده در مقدار معینی از حلال یا محلول تعریف میکنند. آنها در آزمایشگاه با محلولهای گوناگونی سروکار دارند. مقدار حلشونده این محلولها در گسترهای از مقدار بسیار کم تا مقدار بسیار زیاد متغیر است. بهخاطر همین است که غلظت محلولها را به روشهای گوناگون بیان میکنند.
فرم دریافت آموزش های ویدئویی کامل شیمی:
اگه میخوای کل شیمیت رو تو کمترین زمان و با تدریس انیمیشنی مفهومی تستی رتبه 127 کنکور، آقای دکتر متین هوشیار جمع کنی؛ فرم رو پر کن و منتظر تماسمون باش:
روی نمره 20 و درصد بالای 70 شیمی (مثل رتبه های برتر هر سالمون) حساب کن!
برای دسترسی به دیگر درسهای فصل 3 شیمی 10، روی لینک های زیر کلیک کنید: