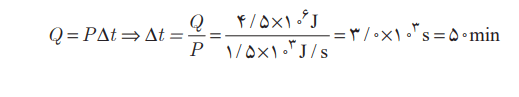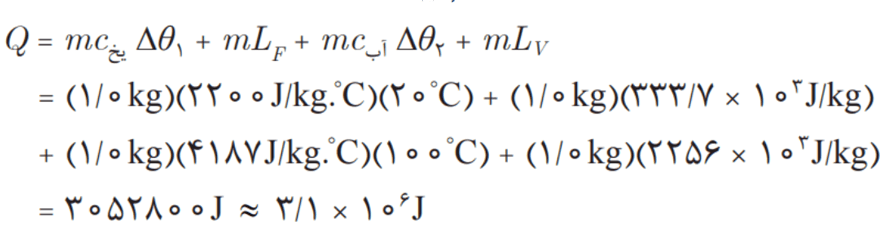آموزش درس 4 فصل 4 فیزیک دهم بهصورت تستبیس، همراه با تدریس ویدیویی «شهاب نصیری» را، در این پست از رپیتیچ ببینید.
در جلسه قبل با اکثر مباحث مرتبط به گرما، مخصوصا دمای تعادل آشنا شدیم. درس چهارم این فصل به تغییر حالتهای ماده اختصاص دارد.
برای دسترسی به کل مباحث فصل چهارم، روی لینک زیر کلیک کنید.
فیلم و جزوه فصل چهارم فیزیک دهم
خب، اول از همه بریم که ویدیوی آموزشی این بخش رو ببینیم.
آموزش ویدیویی درس 4 فصل 4 فیزیک دهم
در این قسمت، بخشی از «آموزش درس چهارم فصل چهارم فیزیک دهم» را بهصورت ویدیویی میتوانید ببینید. مدرس این قسمت، جناب مهندس شهاب نصیری، مولف برتر آزمونهای موسسات معتبر هستند.
فرم دریافت آموزش های ویدئویی فیزیک:
اگه تو هم میخوای کل فیزیکت رو تو کمترین زمان و با تدریس انیمیشنی مفهومی تستی مهندس شهاب نصیری جمع کنی؛ کافیه این فرم رو پر کنی و منتظر تماسمون باشی:
روی نمره 20 و درصد بالای 70 فیزیکت (مثل رتبه های برتر هر سالمون) حساب کن!
تغییر حالتهای ماده در این درس به دو بخش «تغییر حالت جامد-مایع» و «تغییر حالت مایع-بخار» تقسیم میشود. حالت مایع-بخار دارای مباحث بیشتری نسبت به حالت جامد-مایع است. بنابراین زمان بیشتری را برای یادگیری آن باید اختصاص بدهید.
تغییر حالتهای ماده؛ درس چهارم فصل چهارم فیزیک دهم
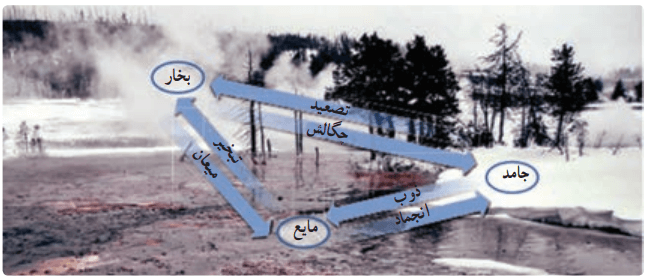
موادی که در اطراف ما وجود دارند، معمولا در سه حالت (فاز) جامد، مایع و گاز (بخار) یافت میشوند. گذار از یک حالت (فاز) به یک حالت (فاز) دیگر را یک تغییر حالت (گذار فاز) مینامند. در شکل پایین انواع تغییر حالتهایی که برای سه حالت آب امکانپذیر است، نشان داده شده است. تغییر حالتها معمولا با گرفتن و یا از دست دادن گرما همراهاند.
تبدیل جامد به مایع را ذوب و تبدیل مایع به بخار را تبخیر میگوییم. تبدیل مایع به جامد، انجماد و تبدیل بخار به مایع، چگالش بخار به مایع یا میعان نام دارد. امکان دارد که تغییر حالت از جامد به بخار بهطور مستقیم و بدون گذر از حالت مایع صورت گیرد. وارون این قضیه یعنی از بخار به جامد نیز امکانپذیر است. تغییر حالت از جامد به بخار، تصعید و تغییر حالت وارون آن، یعنی از بخار به جامد چگالش بخار به جامد نام دارد. برای یادگیری بهتر این شرایط بیایید چند مثال بزنیم. نفتالین در دمای اتاق به طور مستقیم از جامد به بخار تبدیل میشود. در صبحهای بسیار سرد زمستان، برفکی که روی گیاهان و یا روی شیشه پنجره مینشیند را دیدهاید؟ این برفک، بخار آبی است که به طور مستقیم به بلورهای یخ تبدیل شده است.
در ادامه تغییر حالتهای جامد-مایع و مایع-بخار را بهطور جداگانه بررسی میکنیم.
تغییر حالت جامد-مایع
اگر به جسم جامدی گرما دهیم، دمای آن افزایش مییابد. بیایید عمل گرما دادن را برای جامدهای خالص و بلورین ادامه بدهیم. وقتی دمای جسم به مقدار مشخصی برسد، افزایش دما متوقف میشود و دما ثابت باقی میماند. در این حالت، جسم شروع به ذوب شدن میکند و به مایع تبدیل میشود. این دمای ثابت را نقطه ذوب یا دمای گذار جامد به مایع مینامند. نقطه ذوب به جنس جسم و فشار وارد بر آن بستگی دارد. به استثنای چند مورد خاص، حجم جامدهای بلوری هنگام ذوب شدن افزایش مییابد. حجمی که بلور با آرایش منظم مولکولها در حالت جامد اشغال میکند، نسبت به حالت مایع کمتر است. دلیلش این است که در حالت مایع، آرایش مولکولی بلور نامنظم میشود.
جامدهای بیشکل مانند شیشه و جامدهای ناخالص مانند قیر برخلاف جامدهای خالص و بلوریناند. آنها نقطه ذوب کاملا مشخصی ندارند. در واقع وقتی این مواد را گرم میکنیم، پیش از ذوب شدن خمیریشکل میشوند. این مواد در گسترهای از دما بهتدریج ذوب میشوند.
معمولا افزایش فشار وارد بر جسم سبب بالا رفتن نقطه ذوب جسم میشود. با این حال، در برخی موارد مانند یخ این قضیه متفاوت است. افزایش فشار به کاهش نقطه ذوب میانجامد که این در مورد یخ بسیار ناچیز است.
عمل ذوب، فرایندی گرماگیر است. به جسم جامدی که به دمای ذوب خود رسیده باشد، باید گرما بدهیم تا به مایع تبدیل شود. دلیلش این است که مولکولهای جامد باید از ساختار صلب قبلی خود رها شوند. این گرما، دمای جسم را تغییر نمیدهد؛ بلکه سبب تغییر حالت آن میشود. ذوب شدن یک قالب یخ و تبدیل آن به آب، مثالی مشهور از این دست است.
فعالیت 4-6
برف و یخ دو شکل آشنای حالت جامد آب هستند. با وجود این، ظاهر متفاوتی دارند. دلیل این امر را تحقیق کنید.
پاسخ: وقتی دمای محیط در ابتدا بالای نقطه انجماد آب باشد و هوا خنک شود، بخار تبدیل به باران میشود. با سردتر شدن هوا، این آب به شکل تگرگ یخ میزند.
اگر دما در ابتدا زیر نقطه انجماد آب باشد، بخار آب مستقیما از حالت گازی به حالت جامد میرود (چگالش). در این صورت بلورهای یخ معلق در هوا تقارن شش وجهی خود را حفظ میکنند. این بلورها ضمن اینکه به آرامی رشد میکنند، دانههای برف را تشکیل میدهند.
گرمای نهان ذوب
انجماد یک مایع و تبدیل آن به یک جامد، عکس فرایند ذوب شدن است. لازمه این فرایند گرفتن گرما از مایع است تا مولکولها بتوانند در یک ساختار جدید قرار گیرند. در اینجا نیز تغییر حالت بدون تغییر دما رخ میدهد. گرمای منتقل شده برای تغییر حالت جسم از جامد به مایع و برعکس، با جرم جسم نسبت مستقیم دارد. نسبت این گرما به جرم جسم را گرمای نهان ویژه ذوب میگویند. این گرما را به اختصار، گرمای نهان ذوب مینامیم و آن را با LF نشان میدهیم.
گرمای نهان ذوب بستگی به جنس جسم دارد. یکای آن در SI ژول بر کیلوگرم (J/kg) است. وقتی نمونهای به جرم m کاملا تغییر فاز دهد، گرمای منتقل شده برابر با Q=mLF است.
وقتی تغییر فاز از جامد به مایع انجام میشود، جسم گرما میگیرد (0<Q) :
Q = +mLF
و اگر تغییر فاز از مایع به جامد انجام شود، جسم گرما از دست میدهد (0>Q) :
Q = -mLF
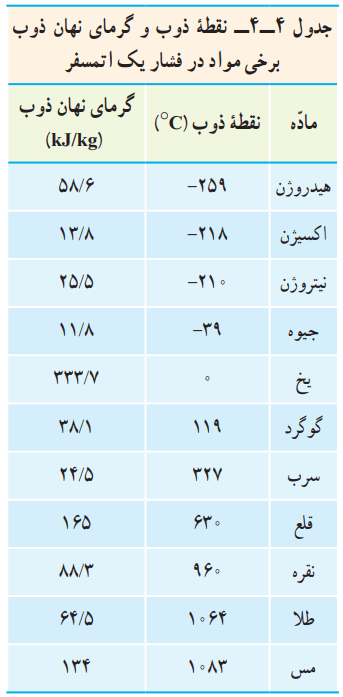
گرمای نهان ذوب و نقطه ذوب مواد مختلف، متفاوت است. این مقدارها برای برخی از مواد در جدول 4-4 داده شده است.
فعالیت 4-7
تحقیق کنید وجود ناخالصی در مایع چه تاثیری بر نقطه انجماد آن دارد.
پاسخ: وجود ناخالصی باعث میشود که مایع، نقطه انجماد مشخصی نداشته باشد. بنابراین، فرایند انجماد در گسترهای از دما رخ میدهد.
وجود ناخالصی موجب کاهش نقطه انجماد میشود. فرض کنید مقداری نمک طعام را روی قطعه یخی بپاشیم. مولکولهای نمک تجزیه شده و مولکولهای آب در اطراف یونها، آنها را هیدراته میکنند. در نتیجه مولکولهای بیشتری از یخ به آب میپیوندند. رفته رفته از حجم یخ کاسته و به آب اضافه میشود. بالا بودن انرژی مولکولهای آب در این حالت، سبب گرفتن گرمای بیشتری از یخ میشود. میشود گفت که در اصطلاح، نقطه انجماد فرو میافتد.
مثال 4-10
فلز گالیم (Ga) یکی از چند عنصری است که در دماهای پایین ذوب میشود. دمای ذوب این فلز 29/8 درجه سانتیگراد و گرمای نهان ذوب آن 8/04kJ/kg است. یک قطعه 10 گرمی از این فلز را در دست خود تصور کنید. این قطعه چقدر گرما از دست ما میگیرد تا در نقطه ذوب خود به طور کامل ذوب شود؟ (از تبادل گرما بین فلز و هوای محیط چشمپوشی شود.)
پاسخ: با استفاده از رابطه 4-10 داریم:
Q = mLF = (10/0 × 10-3kg) (8/04 × 103J/kg) = 804J
مثال 4-11
یک جواهر ساز برای ساختن جواهری میخواهد از 0/500kg نقره برای ریختن در قالبهای جواهر استفاده کند. به این منظور او باید نقره را ذوب کند. فرض کنید دمای اولیه نقره همان دمای اتاق و برابر 20 درجه سانتیگراد باشد. با این حساب چقدر گرما باید به این مقدار نقره داده شود؟
پاسخ: مرحلههای این فرایند بهطور طرحوار در شکل زیر رسم شده است.
که در آن
Q1 = mنقرهcنقرهΔΘ = (0/500kg) (236J/kg.°C) (960°C – 20°C) = 1/11 × 105J
Q2 = mنقرهLF = (0/500kg) (88/3kJ/kg) = 0/442 × 105J
که در آن از گرمای ویژه و گرمای نهان ذوب نقره مندرج در جدولهای 4-3 و 4-4 استفاده کردیم. اکنون گرمای کل با جمع کردن Q1 و Q2 به دست میآبد:
Q = Q1 + Q2 = 1/11 × 105J + 0/442 × 105J = 1/55 × 105J = 155kJ
تغییر حالت مایع-بخار
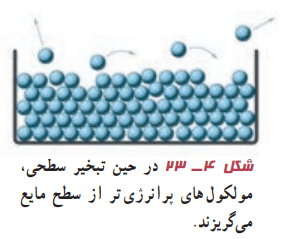
میدانیم که به تبدیل مایع به بخار تبخیر میگویند. خشک شدن سریع یک زمین خیس در هوای گرم تابستان و یا لباس روی بند رخت را درنظر بگیرید. این دو مثالهایی از نوعی تبخیر هستند که به آن تبخیر سطخی میگویند. تا پیش از رسیدن به نقطه جوش مایع، تبخیر بهطور پیوستهای از سطح مایع رخ میدهد. در پدیده تبخیر سطحی، تندی برخی از مولکولهای مایع به حدی میرسد که میتوانند از سطح مایع فرار کنند.
آهنگ رخ دادن این فرایند به عواملی از جمله دما و مساحت سطح مایع بستگی دارد.
فعالیت 4-8
الف) بررسی کنید از دیدگاه مولکولی، افزایش دما و افزایش مساحت سطح مایع چگونه بر آهنگ تیخیر سطحی مایع اثر میگذارد؟
پاسخ: با افزایش سطح، تعداد ذراتی که با سطح در ارتباط هستند بیشتر شده و نرخ تبخیر سطحی بالاتر میرود. افزایش دم باعث افزایش انرژی جنبشی و تندی ذرات میشود. در نتیجه ذرات، انرژی بیشتری برای فرار از سطح مییابند و نرخ تبخیر سطحی بالا میرود.
ب) سعی کنید تبخیر سطحی را در شرایط مختلف بررسی کنید. از راه تجربه بگویید که چه عوامل دیگری بر روی آهنگ تبخیر سطحی موثر هستند.
پاسخ: نوع مایع مورد نظر – فشار هوا
پ) تحقیق کنید که کوزههای چگونه میتوانند آب داخل خود را خنک کنند.
پاسخ: در این کوزهها مقداری عمل تبخیر صورت میگیرد. گرمای مورد نیاز این تبخیر از کوزه گرفته میشود. در نتیجه دمای خود کوزه پایین آمده و آب درون آن خنک میماند.
فرایند جوشیدن
وقتی مایعی را روی اجاقی قرار میدهیم، با گرم کردن مایع به دمای مشخصی میرسیم. در این دما حبابهای گاز از درون مایع بالا میآیند. این مرحله نشانهای از آغاز فرایندی موسوم به جوشیدن است. به این دمای مشخص، نقطه جوش میگویند.
در مورد آب، به محض اینکه حبابها بالا میآیند به آب کمی سردتر میرسند. پیش از رسیدن به سطح آزاد آب با صدای تیزی فرومیپاشند و در آنجا دوباره به مایع تبدیل میشوند. وقتی دمای آب همچنان بالا برود، حبابها میتوانند بیشتر بالا بروند. سرانجام به سطح آزاد آب میرسند و در آنجا با صدای دیگری که به آن «غلغل کردن» میگویند فرومیپاشند.
در این حالت است که میگوییم آب به «جوش کامل» رسیده است. در جوش کامل آهنگ تبخیر به بیشترین مقدار خود میرسد. دماسنجی که مخزن آن درون آب قرار دارد، دمای ثابتی را نشان میدهد. این مقدار برای آب خالص در فشار جوّ متعارف (1atm)، 100 درجه سانتیگراد است.
در جوشیدن، کل مایع در فرایند تبخیر شرکت میکند. به فرایند تبخیر تا پیش از رسیدن به نقطه جوش، تبخیر سطحی میگویند. فرایند تبخیر در نقطه جوش نیز، در اصطلاح جوشیدن نام دارد. به عبارت دیگر، هر دو فرایند تبخیر هستند.
فعالیت 4-9
از تفاوت نقطه جوش اجسام مختلف در صنعت، استفاده زیادی میشود. تحقیق کنید چگونه از این ویژگی برای جدا کردن محصولات نفتی استفاده میشود؟
پاسخ: با افزایش دما، مواد مورد نظر به دمای جوش خود میرسند و تبدیل به بخار میشوند. در این میان با بخار شدن نفت، بخار آن را با فرایند میعان به نفت مایع تبدیل میکنند.
گرمای نهان تبخیر
تجربه نشان میدهد که گرمای منتقل شده برای تبخیر هر مایع با جرم آن نسبت مستقیم دارد. نسبت این گرما به جرم مایع بخار شده را گرمای نهان ویژه تبخیر مینامیم. برای سادگی میشود به آن، گرمای نهان تبخیر گفت که با LV نشان داده میشود.
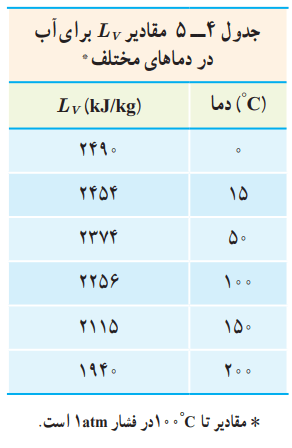
گرمای نهان تبخیر هر مایع به جنس و دمای آن بستگی دارد. یکای آن در SI ژول بر کیلوگرم (J/kg) است. جدول 4-5 برخی از مقدارهای LV را نشان میدهد. این مقادیر به طور تجربی برای آب در دماهای مختلف به دست آمده است.
مایعی به جرم m که گرمای تبخیر آن LV است را درنظر بگیرید. گرمای لازم برای تبخیر آن از رابطه زیر به دست میآید:
Q = +mLV
علامت مثبت نشان دهنده آن است که مایع هنگام تبخیر گرما میگیرد.
پرسش 4-4
چرا در جدول 4-5 گرمای نهان تبخیر آب با افزایش دمای آن کاهش مییابد؟
پاسخ: با افزایش دما جنبش مولکولها افزایش یافته و پیوند بین آنها سستتر میشود. با این روند، مولکولها برای جدا شدن از سطح به انرژی کمتری نیاز دارند. بنابراین با افزایش دمای آب، گرمای کمتری برای تبخیر آن نیاز است.
مثال 4-12
میشود هوا را با بخاریهای شعلهای گرم کرد. برای حفظ رطوبت محیط در این روش، معمولا ظرف آبی را روی بخاری میگذارند. فرض کنید دمای آب در یکی از این ظرفها روی 50 درجه سانتیگراد ثابت مانده باشد. تعیین کنید برای نبخیر 0/200kg از آب در این شرایط چقدر گرما لازم است؟
پاسخ: با توجه به رابطه 4-11 و استفاده از جدول 4-5 داریم:
Q = +mLV = +(0/200kg) (2374 × 103J/kg) = 4/75 × 105J
گرمای نهان تبخیر مابع در نقطه جوش
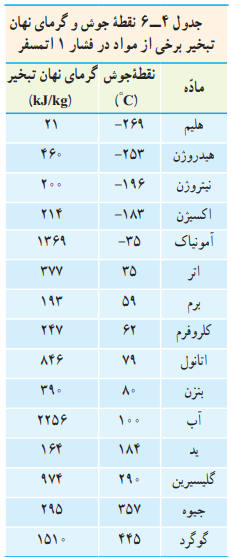
در مسئلههای عملی بیشتر با گرمای نهان تبخیر مایع در نقطه جوش آن سروکار داریم. البته نقطه جوش هر مایع به جنس و فشار وارد بر آن بستگی دارد. افزایش فشار وارد بر مایع سبب بالا رفتن نقطه جوش آن میشود. جدول 4-6 نقطه جوش و گرمای نهان تبخیر مربوط به این نقطه را برای برخی از مواد در فشار 1 اتمسفر نشان میدهد.
برای اندازهگیری گرمای نهان تبخیر در نقطه جوش هر مایع، روشهای عملی گوناگونی وجود دارد.
پرسش 4-5
الف) چرا غذا در دیگ زودپز، زودتر پخته میشود؟
پاسخ: با محبوس بودن زودپز، فشار دورن دیگ بالا میرود. افزایش فشار باعث بالا رفتن دما شده که موجب میشود غذا زودتر بپزد.
ب) دلیل دیرتر پخته شدن تخممرغ در ارتفاعات چیست؟ کوهنوردان برای رفع این مشکل چه کاری انجام میدهند؟
پاسخ: در ارتفاعات فشار هوا کاهش مییابد. در نتیجه دمای جوش آب پایین میآید که موجب دیرتر پخته شدن تخممرغ میشود. کوهنوردان برای رفع این مشکل از ظروف دربسته استفاده میکنند. این ظروف باعث بالا رفتن فشار و دمای جوش میشوند.
مثال 4-13
2 لیتر آب را درون یک کتری برقی با توان الکتریکی 1/5kW میریزیم و آن را روشن میکنیم.
الف) از شروع جوشیدن تا تبخیر همه آب درون کتری چقدر گرما به آب داده میشوذ؟
ب) چه مدت طول میکشد تا این فرایند انجام شود؟ فرض کنید تمام انرژی الکتریکی تبدیل شده به انرژی گرمایی، به آب میرسد.
پاسخ:
الف) با توجه به رابطه 4-11 و جدول 4-6 داریم:
Q = mLV = +(2/0kg) (2256 × 103J/kg) = 4/5 × 106J
ب) آنگاه با استفاده از رابطه توان خواهیم داشت:
تمرین 4-6
قطعه یخی به جرم 1/0kg و دمای اولیه 20- درجه سانتیگراد را گرم میکنیم. عمل گرما دادن را آنقدر ادامه میدهیم تا تمام آن تبدیل به بخار 100 درجه سانتیگراد شود. کل گرمای مورد نیاز برای این تبدیل چند کیلو ژول است؟
پاسخ: ابتدا بهطور طرحوار مشخص میکنیم که قطعه یخ باید چندبار تغییر حالت بدهد:
حالا طبق محاسبات زیر، میتوان به جواب رسید:
پدیده میعان
تبدیل بخار به مایع نیز در طبیعت رخ میدهد و گاهی قطرههای مایعی از بخار روی سطوح جامد تشکیل میشود. به این پدیده، میعان میگویند. در واقع میعان، وارون فرایند تبخیر است. بنابراین، بخار گرما از دست میدهد و به مایع تبدیل میشود.
مقداری بخار به جرم m و گرمای نهان تبخیر LV را درنظر بگیرید. گرمای مربوط به میعان آن از رابطه زیر به دست میآید:
Q = -mLV
علامت منفی نشان دهنده آن است که بخار هنگام میعان گرما از دست میدهد. در نتیجه باعث گرم شدن اجسام پیرامون خود میشود. دقت کردهاید که در مناطق شرجی و دارای رطوبت زیاد، احساس گرمای بیشتری میکنید؟ دلیل آن، میعان بخار آب روی بدن است.
فعالیت 4-10
در مورد ایجاد شبنم صبحگاهی روی گیاهان تحقیق کنید.
پاسخ: دمای هوا هنگام طلوع خورشید پایین است. سطوح شاخه و برگ گیاهان به قدری سرد میشوند که بخار آب با برخورد به آنها، گرمای خود را از دست میدهد. در نتیجه، طی فرایند میعان باعث ایجاد شبنم صبحگاهی میشود.
مثال 4-14
یک روز سرد زمستانی را درنظر بگیرید. بخار آب موجود در اتاقی روی شیشه پنجره به شکل مایع درمیآید و قطرهقطره میشود. فرض کنید دمای شیشه حدود 0 درجه سانتیگراد باشد. برای آنکه 50g آب روی شیشه تشکیل شود، چقدر گرما به شیشه داده میشود؟
پاسخ: با استفاده از جدول 4-6 و رابطه 4-11 داریم:
Q = -mLV = -(50 × 10-3kg) (2490 × 103J/kg) = -1/2 × 105J
در این عمل، 1/2 × 102 کیلو ژول گرما به شیشه داده میشود.
فعالیت 4-11
در فرایندهای تغییر حالت (تغییر فاز) دما تغییر نمیکند. با این حال، انرژی درونی ماده تغییر میکند. در این باره تحقیق کنید.
پاسخ: گرمای داده شده در این حالت، باعث افزایش انرژی جنبشی و پتانسیل، یعنی باعث افزایش انرژی درونی میشود. بیایید از دیدگاه میکروسکوپیک این قضیه را بررسی کنیم. با ادامه روند گرما دادن به ماده، جنبوجوش ذرات آن بالا رفته و پیوند میان آنها سست میشود. این موضوع خود را به صورت افزایش انرژی پتانسیل نشان میدهد.
انرژی درونی، مجموع انرژیهای جنبشی همه اتمها و مولکولهای تشکیلدهنده جسم است. انرژی پتانسیل مولکولی هم مربوط به برهمکنشهای اتمها و مولکولهای آنهاست. وقتی جسم گرم میشود، انرژی جنبشی ذرات تشکیلدهنده آن افزایش مییابد. بنابراین، انرژی درونی آن بیشتر میشود.
در زمان تغییر حالت ماده، گرمای داده شده صرف غلبه بر نیروهای بین مولکولی میشود. با این حساب، انرژی جنبشی متوسط مولکولها تغییر نمیکند و دما ثابت میماند. با از بین رفتن نیروهای بین مولکولی، انرژی پتانسیل آنها افزایش مییابد و انرژی درونی بیشتر میشود.
فرم دریافت آموزش های ویدئویی فیزیک:
اگه تو هم میخوای کل فیزیکت رو تو کمترین زمان و با تدریس انیمیشنی مفهومی تستی مهندس شهاب نصیری جمع کنی؛ کافیه این فرم رو پر کنی و منتظر تماسمون باشی:
روی نمره 20 و درصد بالای 70 فیزیکت (مثل رتبه های برتر هر سالمون) حساب کن!
برای دسترسی به دیگر درسهای فصل 4 فیزیک 10، روی لینک های زیر کلیک کنید: